免疫チェックポイント阻害剤はT細胞のアポトーシスを探求するところから始まった!
今日はT細胞とがん細胞の結合を遮断する免疫チェックポイント阻害剤について、その仕組みをより具体的に見て行こうと思います。
免疫チェックポイント阻害剤の開発に関わったのは、2018年ノーベル医学生理学賞に輝いた京都大学の本庶佑教授と米国テキサス大学のジェームス・アリソン教授で、その研究は、それまでの免疫療法の中心であった、免疫を活性化させる方法とは逆の、免疫を抑える分子(免疫チェックポイント分子)のがん細胞との関りを探るところからでした。
従来の免疫療法と言えば、インターフェロンαやインターロイキン2と言った、サイトカイン療法やがんワクチンなど、免疫を増強して癌細胞を直接攻撃するものでした。
これに対し、本庶先生たちは、免疫応答を制御する免疫チェックポイント分子に目をつけ、自己を攻撃しないためや過剰に活性化しないためにT細胞を抑制することで、結果的にがん細胞を攻撃する免疫チェックポイント阻害剤にたどりついたのです。
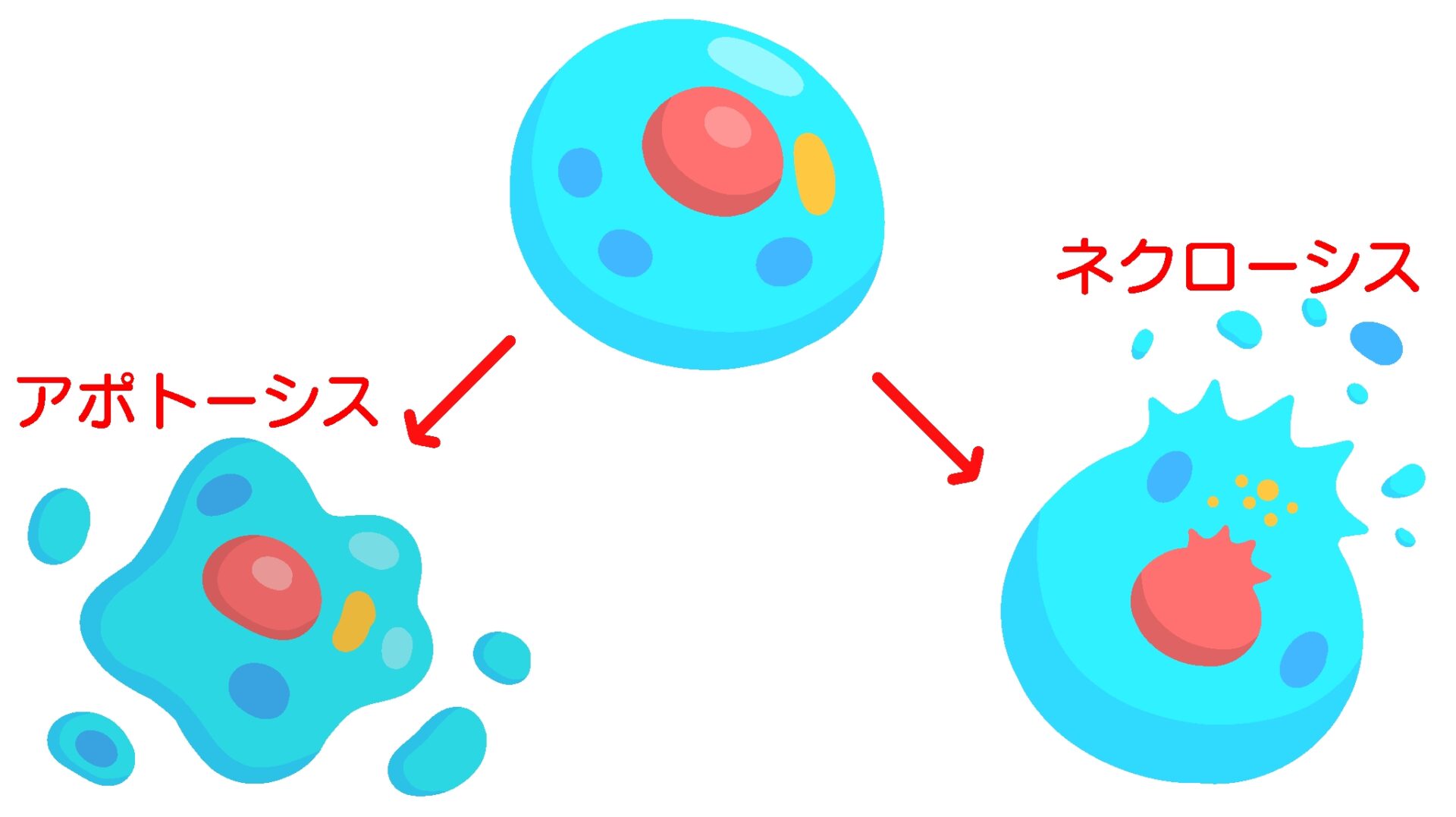
まずは、T細胞に生じるアポトーシス(細胞死)の解明から、獲得免疫のT細胞は異物排除の役割を終えると抗原情報を記憶する細胞だけを残し、アポトーシスによって自ら消滅します。
この際、どのようにしてT細胞がアポトーシスを生じるかを探求し、活性化したT細胞に発現する遺伝子、PD-1(Programmed cell death-1 :プログラム細胞死タンパク質1)を発見しました。
このPD-1こそ、免疫チェックポイント阻害剤における、T細胞とがん細胞の結合部分である、T細胞側の‟手”になります。
そして、このPD-1が、がん細胞側の表面にありPD-1との結び‟手”となる、PD-L1という刺激分子と結合すると、T細胞の機能が抑えられることを突き止めました。
要するに、この2つの結び手の部分を遮断することで、がん細胞を結果的に攻撃しようと考えたものが、免疫チェックポイント阻害剤という形で、免疫療法につながっていきました。
この続きはまた、明日お伝えします。

コメント